2017年10月17日,北京市食品药品监督管理局对北京博辉瑞进生物科技有限公司的动物源类医用生物疝修补片及一次性使用包皮切割吻合器两项产品,进行了为时两天的医疗器械生产质量管理规范现场考核。整个检查由药监局审核组组长王子佳带队,共4名审查员,分为审核首次会议、生产车间现场考核、文件及记录审核、审核末次会议四个环节。
当日上午,考核组组长王子佳组织审核首次会议,宣布两天的检查项目、流程及时间安排。会上,博辉瑞进公司CEO李学军发言,欢迎审查组老师莅临检查并介绍了公司生产经营状况,要求接受检查的部门人员全力配合审查组老师的严格审查;
下午,审查组成员按照会议进程,组织相关人员对公司的生产车间进行了细致全面的现场考核。
次日,审查组成员针对本次考核内容涉及的文件和记录进行了严格审查,且给出专业的指导建议。此次GMP认证,公司质量部、生产部、研发部等相关部门及人员准备充分,经过2天紧张忙碌的严格审查,审查组组长在18日下午的审核末次会议上郑重宣布了博辉瑞进公司顺利通过了GMP的认证审核。
这次GMP认证的顺利通过,使博辉瑞进公司在医疗器械生产质量管理方面更加标准化和规范化,促进我公司在医疗器械领域的飞速发展。

对一个家庭来说,最大的喜事之一,莫过于添...

截止目前,全球已有十余款新冠疫苗在多个国...

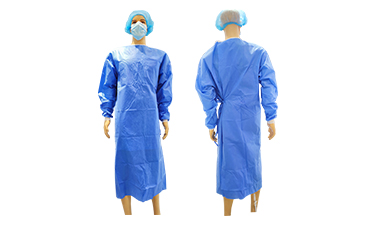
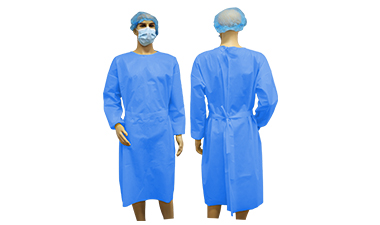
产品名称:新型冠状病毒(2019-nC...

正文...

南德 TÜV CE证书编号:No.G2...

南德 TÜV CE证书编号:No.G2...
南德 TÜV CE证书编号:No. G...

南德 TÜV CE证书编号:No.G2...

南德 TÜV CE证书编号:No. G...
南德 TÜV CE证书编号:No. G...
版权所有北京博辉瑞进生物科技有限公司 京ICP备16026579号 (京)-非经营性-2017-0030  京公网安备 11011502006176号 (京)网药械信息备字(2022)第00096号
京公网安备 11011502006176号 (京)网药械信息备字(2022)第00096号