近日,博辉瑞进旗下III类医疗器械产品硬脑(脊)膜修补片成功通过越南卫生部审核,获批越南D类医疗器械注册证。这标志着该产品已具备越南市场的准入资格,可在当地开展销售与临床应用,不仅拓宽了企业在东南亚市场的布局,也为国产高端植入医疗器械“走出去”提供了重要借鉴。

据了解,越南将医疗器械按风险等级分为A至D四类,其中D类为最高风险等级,主要涵盖植入式医疗器械、生命支持类设备等关键品类。该类产品的注册审批需通过越南卫生部全流程严格审查,对产品的安全性、有效性、企业质量管理体系、生产合规性等都有严苛的考核标准。此次博辉瑞进硬脑(脊)膜修补片成功获批越南D类医疗器械注册证,不仅充分印证了博辉瑞进产品在安全性与临床有效性上的过硬品质,同时体现了博辉瑞进的质量管理体系、生产标准、风险管控等环节均已达到国际水准。
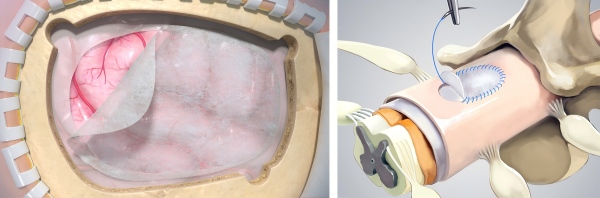
作为博辉瑞进的核心产品之一,此次获批的硬脑(脊)膜修补片采用博辉瑞进自主创新研发的SIS生物材料制备而成。该产品具有多重优势:可应用于多种神经外科手术场景,有效预防脑脊液渗漏并发症的发生;力学强度适宜,方便临床操作使用;材料本身含有丰富生物活性因子,可内源性诱导组织再生,且随组织再生可同步吸收完全降解;优良的耐受感染性能,是临床理想的硬脑(脊)膜修复替代材料。

《中国肺癌杂志》2024年6月第27卷第...

2024年12月6日,为期三天的SDHE...

理智弄槽外科韵,巴山蜀水天府情。2024...

近日,《中华胸心血管外科杂志》2024年...

2024年5月9日,在VBEF未来医疗生...

新春伊始,万象更新。博辉瑞进迎来新春“开...
版权所有北京博辉瑞进生物科技股份有限公司 京ICP备16026579号 (京)-非经营性-2017-0030  京公网安备 11011502006176号 药品医疗器械网络信息服务备案(京)网药械信息备字(2022)第00096号
京公网安备 11011502006176号 药品医疗器械网络信息服务备案(京)网药械信息备字(2022)第00096号